Hari, tanggal : Senin, 15 oktober 2012
I. Tujuan
I. Tujuan
- Mengidentifikasi
senyawa asam karboksilat dan ester
- Mempelajari sifat fisik dan kelarutan dari senyawa tersebut
- Mempelajari cara pembuatan ester (esterifikasi)
II. Dasar Teori
- Mempelajari sifat fisik dan kelarutan dari senyawa tersebut
- Mempelajari cara pembuatan ester (esterifikasi)
II. Dasar Teori
Suatu
asam karboksilat adalah suatu senyawa organik yang mengandung gugus karboksil, –COOH. Gugus karboksil mengandung gugus karbonil dan sebuah
gugus hidroksil; antar aksi dari kedua gugus ini mengakibatkan suatu
kereaktifan kimia yang unik dan untuk asam karboksilat (Fessenden,
1997).
Asam
format terdapat pada semut merah (asal dari nama), lebah, jelatang dan
sebagainya (juga sedikit dalam urine dan peluh). Sifat fisika: cairan,
tak berwarna, merusak kulit, berbau tajam, larut dalam H2O dengan sempurna. Sifat kimia: asam paling kuat dari asam-asam karboksilat, mempunyai gugus asam dan aldehida (Riawan, 1990).
Asam asetat (CH3COOH) sejauh
ini merupakan asam karboksilat yang paling penting diperdagangan,
industri dan laboratorium. Bentuk murninya disebut asam asetat glasial
karena senyawa ini menjadi padat seperti es bila didinginkan. Asam
asetat glasial tidak berwarna, cairan mudah terbakar (titik leleh 7ºC,
titik didih 80ºC), dengan bau pedas menggigit. Dapat bercampur dengan
air dan banyak pelarut organik (Fessenden, 1997).
Adapun sifat-sifat yang dimiliki oleh asam karboksilat adalah:
1. Reaksi Pembentukan Garam
2. Reaksi Esterifikasi
3. Reaksi Oksidasi
4. Pembentukan Asam Karboksilat
Esterifikasi adalah salah satu jenis reaksi dimana reaksi tersebut untuk menghasilkan ester. Ester merupakan sebuah hidrokarbon yang diturunkan dari asam karboksilat. Sebuah asam karboksilat mengandung gugus -COOH, dan pada sebuah ester hidrogen di gugus ini digantikan oleh sebuah gugus hidrokarbon dari beberapa jenis. Ester dapat dihasilkan dengan cara mereaksikan antara sebuah alcohol dengan asam karboksilat yang dapat dituliskan sebagai berikut :
RCOOH + R’OH → RCOOR + H2O
Pentingnya kita melaksanakan praktikum
esterifikasi didasarkan pada sifat-sifat reaksi esterifikasi yang khas
yaitu sifat reaksi yang reversible/dapat balik, bersifat sangat lambat.
Hal-hal inilah yang nantinya akan kita jadikan variable percobaan
untuk mengetahui bagaimana pembentukan ester yang optimal.Aplikasi pembentukan ester sangatlah banyak di industry. Misalkan dalam proses dasar saat pembuatan plastic, senyawa aroamatik dan lain-lain. Oleh karena itu ita perlu untuk mempelajari reaksi esterifikasi dalam skala laboratorium dan mengetahui aplikasinya di Industri.
Esterifikasi
Macam-macam reaksi esterifikasi yaitu antara lain
- Reaksi antara asam karboksilat dengan suatu alcohol
- Reaksi antara asil klorida dengan alcohol atau fenol
- Reaksi antara suatu anhidrida asam dengan fenol
III. Alat dan Bahan
Alat :- Tabung reaksi
- Penaggas
- Beaker glass
- Pipet
- Termometer
Bahan :
- Asam Salisilat 0,5 garm
- Aquadest
- NaOH 3M
- HCL 3M
- Es Batu
- Etanol 70 % 3ml
- Butanol 3 ml
- Asam Asetat
- H2SO4
IV. Cara Kerja
a. Asam Karboksilat
b. Esterifikasi
V. Hasil Pengamatan
1. Asam karboksilat
2. Esterifikasi
VI. Pembahasan
Praktikum kali ini bertujuan untuk mengetahui serta memahami
reaksi-reaksi gugus karboksilat dalam suatu senyawa. Percobaan pertama yaitu mengidentifikasi reaksi
yang terjadi pada asam karboksilat.
Percobaan ini dimulai dengan memasukkan 0,5 gr asam
salisilat ke dalam tabung reaksi yang berisi 5 ml air dingin, kemudian dikocok
agar larutan menjadi homogen. Hasil yang diperoleh adalah padatan asam
salisilat tidak larut dalam air dingin. Asam salisilat yang tidak larut
tersebut dipanaskan hingga mulai mendidih, hasil yang didapatkan adalah padatan
asam salisilat yang tidak larut membentuk kristal.
Selanjutnya
kristal yang terbentuk di dalam tabung reaksi didinginkan didalam gelas beaker
menghasilkan asam salisilat yang mengkristal memadat menjadi beku membentuk
endapan putih, namun ketika campuran larutan tersebut ditambahkan 70 tetes
larutan NaOH 3M, endapan putih yang terbentuk menjadi larut. Selanjutnya
larutan tersebut ditambahkan HCl 2M sebanyak 70 tetes , penambahan sebanyak 70
tetes ini bertujuan menyamakan tetesan yang ditambahkan sewaktu menambahkan
NaOH yang kemudian ditambahkan 10 tetes HCl lagi kedalam larutan tersebut,
hasil akhir yang diperoleh adalah terbentuk kembali endapan putih kristal yang
memadat.
Percobaan
selanjutnya, yaitu mengetahui reaksi-reaksi gugus karboksilat dalam
suatu senyawa dengan
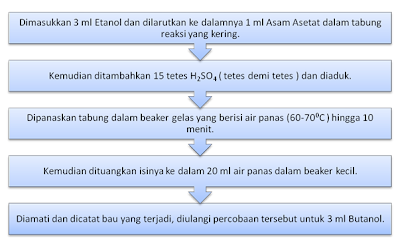
identifikasi reaksi Esterifikasi. Langkah pertama yang perlu dilakukan adalah dimasukkan ke dalam tabung reaksi 3 ml etanol 70% lalu ditambahkan 1 ml asam asetat dan 15 tetes H2SO4
pekat Kemudian dikocok agar larutan homogen dan dipanaskan dalam
penangas air selama 5 menit, pemanasan dilakukan untuk mempercepat
reaksi yang berlangsung. Maka didapatkan sebagai berikut pada sampel
asam format warna larutan bening, ada gelembung, setelah dipanaskan bau
menyengat. Sampel asam propionat warna larutan bening, setelah dipanaskan tetap bau sangat menyengat. Sampel asam asetat warna larutan bening, setelah dipanaskan bau menyengat.
Percobaan tersebut diketahui bahwa asam propionat lebih reaktif
daripada sampel yang lain, karena menghasilkan bau yang sangat
menyengat. Sampel asam asetat yang paling tidak bereaksi.
Langkah kedua yang perlu dilakukan adalah dimasukkan ke dalam tabung reaksi 3 ml butanol lalu ditambahkan 1 ml asam asetat dan 15 tetes H2SO4
pekat Kemudian dikocok agar larutan homogen dan dipanaskan dalam
penangas air selama 5 menit, pemanasan dilakukan untuk mempercepat
reaksi yang berlangsung. Maka didapatkan sebagai berikut pada sampel
asam format ada gelembung, setelah dipanaskan bau menyengat. Sampel asam
propionat warna larutan bening, ada 2 lapisan (atas bening, bawah
kuning) setelah dipanaskan tetap bau menyengat. Sampel asam asetat warna larutan bening, setelah dipanaskan bau tidak
menyengat. Percobaan tersebut diketahui bahwa asam propionat lebih
reaktif dari pada sampel yang lain, karena menghasilkan bau yang
menyengat. Asam asetat paling tidak bereaksi.
Butanol baunya adalah
bau balon dan sedikit bau asetat (menyengat). Sedangkan pada etanol absolut berbau balon (keton) saja. Hal ini disebabkan pada
etanol 70% terdapat 30% air, yang berfungsi sebagai pengikat air,
sehingga ketika larutan dituangkan ke air menghasilkan bau yang
menyengat.
Reaksi Esterifikasi.
C2H5OH + CH3COOH
------->  +
H2O
+
H2O
 +
H2O
+
H2OVII. Kesimpulan
- Percobaan reaksi garam karboksilat terjadi reaksi positif dari asam salisilat karena terjadi perubahan pada saat pemanasan, dengan terbentuknya endapan kristal putih.
- Percobaan esterifikasi, dengan etanol diketahui sampel asam propionat lebih reaktif dari pada sampel yang lain, karena menghasilkan bau yang sangat menyengat. Asam asetat yang paling tidak bereaksi.
VIII. Daftar Pustaka
http://pkimorg1a.blogspot.com/
http://annisanfushie.wordpress.com/2009/01/02/asam-karboksilat/
http://chemical-engineer.digitalzones.com/biodiesel.html
http://group1bprakkimorg.blogspot.com/2012/10/percobaan-ii.html
http://group4kimorg.blogspot.com/2012/11/identifikasi-asam-karboksilat-dan-ester.html
http://pkimorg1a.blogspot.com/ IX. Lampiran
1. Sebutkan cara cara produksi ester selain esterifikasi! Reaski transesterifikasi dari Asam lemak dari minyak lemak nabati direaksikan dengan alkohol menghasilkan ester dan produk samping berupa gliserin.
2. Mengapa HCl pekat dan NaOH tidak bisa menjadi katalis dalam reaksi esterifikasi? Karena HCl dan NaOH tidak dapat mendonorkan 2 proton pada saat mekanisme esterifikasi yaitu proses protonasi.
3. Mengapa setelah penambahan HCl ion salisilat menjadi tidak larut? karena HCl berfungsi untuk mengetahui banyaknya NaOH yang tersisa dalam proses saponifikasi. Disamping itu penambahan HCl juga untuk memberikan suasana asam, karena hasil mula-mula dari reaksi saponifikasi adalah berupa karboksilat, dengan adanya penambahan HCl ini karboksilat diubah menjadi asam karboksilat.
4. Tuliskan persamaan reaksi!
Reaksi asam karboksilat :
C6H7O3 + NaOH →
C7H5NaO3 + H2O
NaOH sisa + HCl
→ NaCl + H2O
+ HCl sisa
Reaksi esterifikasi :
*membuat asetil asetat
CH3CH2OH +
CH3COOH → CH3COOCH2CH3 +
H2O



Tidak ada komentar:
Posting Komentar